1. Cấu trúc tiếp hợp của tế bào và ECM
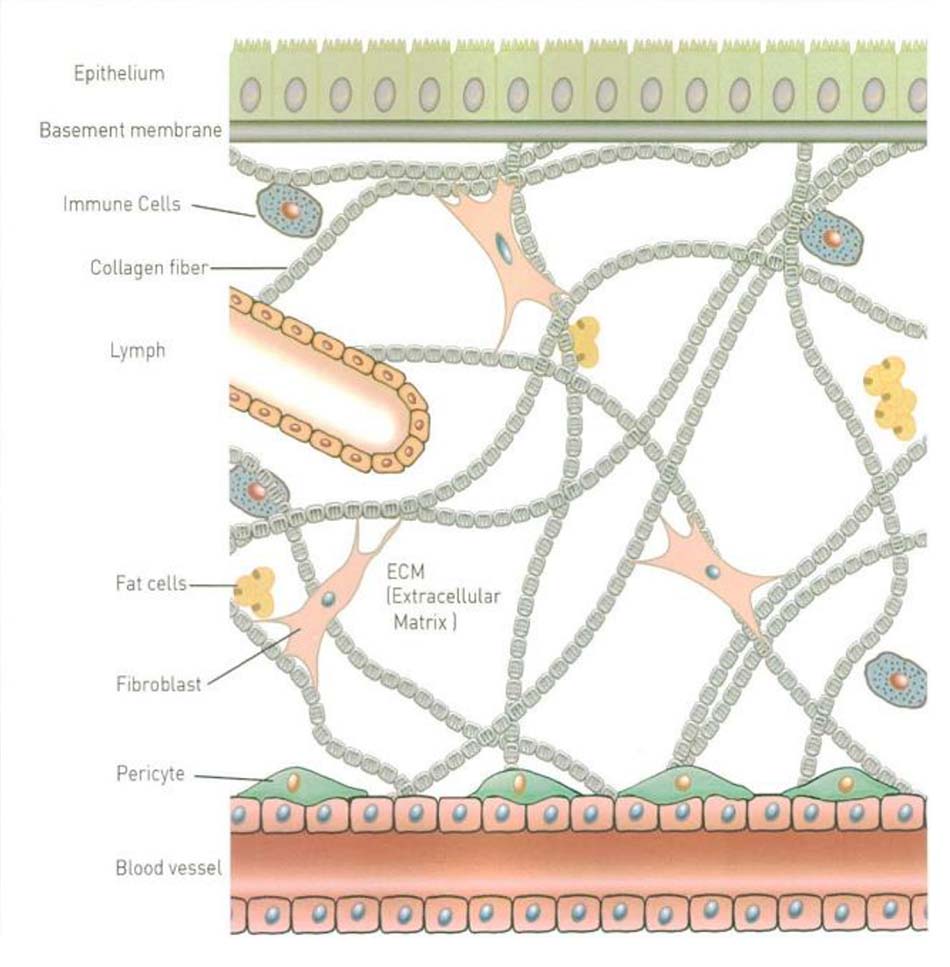
Trong chất nền ngoại bào ECM các Fibroblast (nguyên bào sợi) gần như không có và giữa các fibroblast có khoảng trống giữa các tế bào giữa các nguyên bào sợi, đây là khối Protein được tạo thành bởi polysaccharide, fibrous protein và đóng vai trò trong việc làm vật đệm cho các áp lực phát sinh từ bên ngoài. ECM có thể được chia thành interstitial matrix và basement membrane (màng đáy). Basement membrane đóng vai trò trụ cột trong việc giúp cho các tế bào hoạt động, giả sử nếu tế bào rơi ra khỏi basement membrane thì tế bào sẽ không còn tín hiệu sinh tồn và chết.
Protein được sử dụng khi kết hợp nhóm matrix với tế bào hay tế bào với tế bào được gọi là tế bào bám dính phân tử, có các loại như sau:
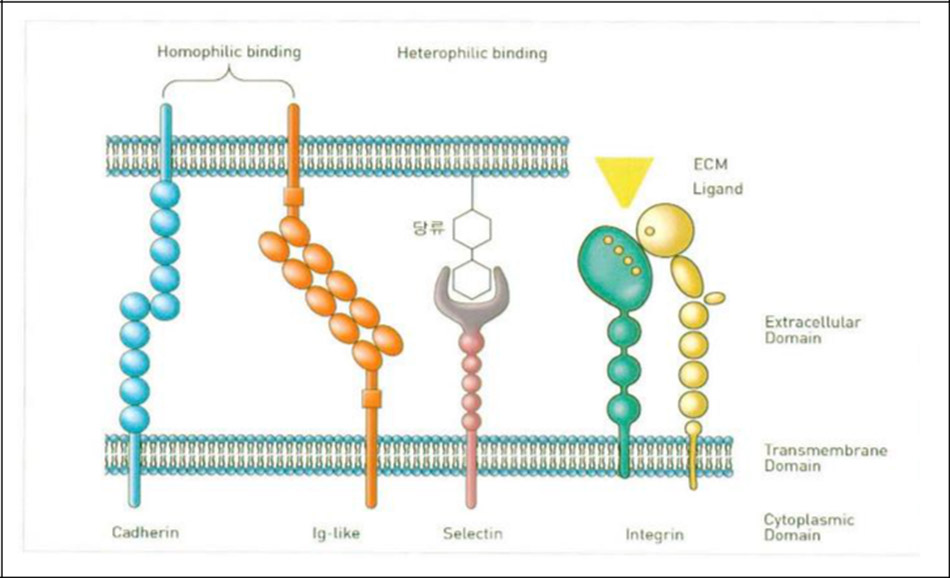
(1) Cadherin (Calcium Dependent Adhering Protein)
Có 12 loại bao gồm Cadherin N.P,R,B,E tác dụng với Actin cytoskeleton, và có Desmocollins và Desmogleins liên quan đến Desmosome.
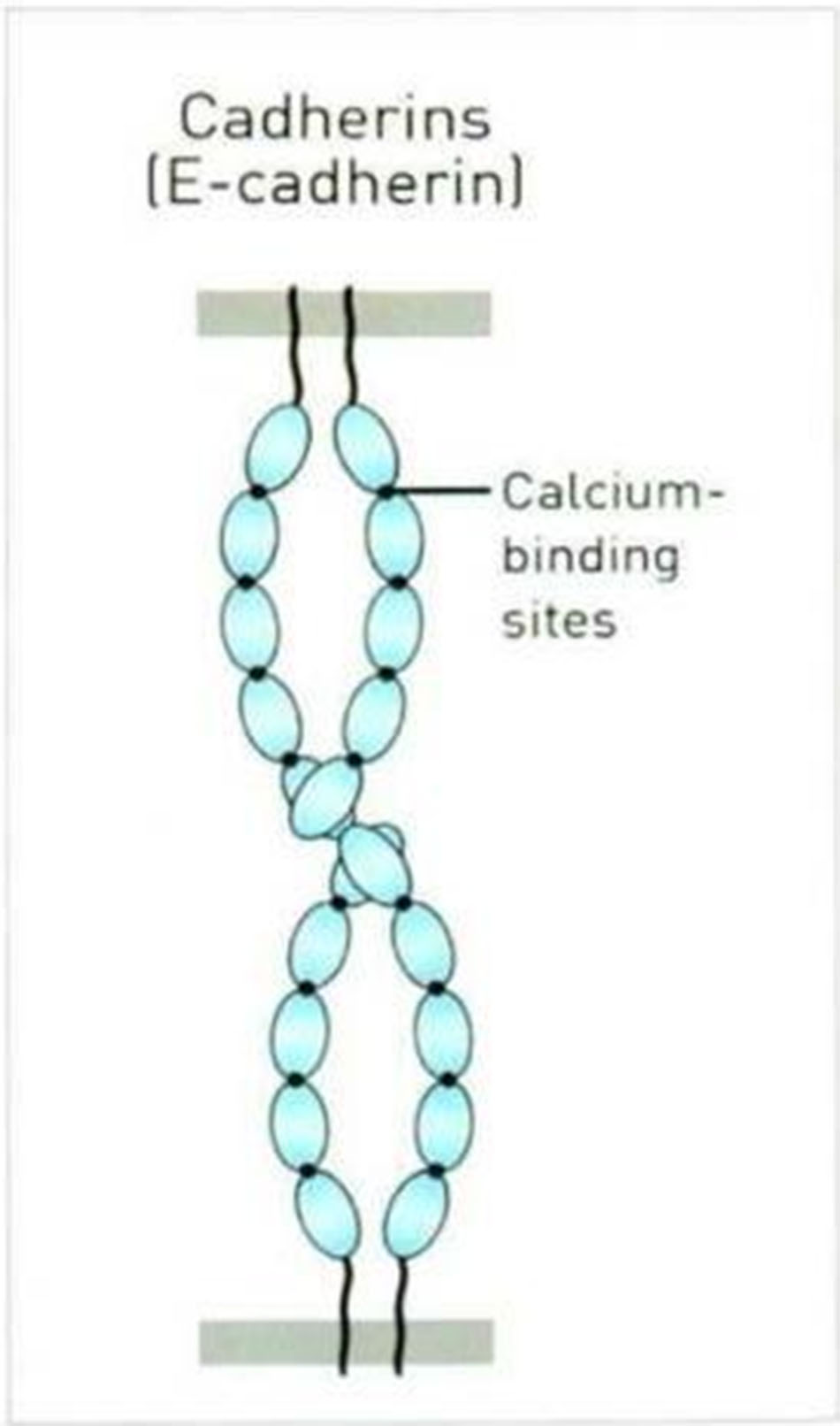
Cadherin là một liên kết ba chiều sử dụng canxi (nghĩa là để loại bỏ Cadherin, chỉ loại bỏ các ion canxi. Các ion canxi có thể được loại bỏ bằng EDTA, EGTA, v.v.) Cadherin được gọi là ctyoplasmic domain, transmembrane domain, extracellular domain, Alpha catenin, beta catenin và p-120 catenin ton tại trong ctyoplasmic domain.
Cadhenin có một số chức năng, chẳng hạn như thực bào khi các tế bào liên kết và ảnh hưởng đến sự truyền tín hiệu bằng betacatenin khi matrix và các tế bào liên kết. Trong nuôi cấy tế bào, các tế bào được nuôi cấy trong thủy tinh và khi tất cả các tế bào được phát triển, chúng có thể được loại bỏ sau khi loại bỏ canxi bằng EDTA và trypsin.. Vài lần như vậy, tế bào có thể được nuôi cấy nhiều lần. Khi tế bào được nuôi cấy trên plate, phần mà tế bào tiếp xúc với kính được gọi là tiếp xúc tiêu cự. Đầu tiên, fibronectin được tiết ra từ huyết tương hoặc các tế bào được chèn vào trước khi nuôi cấy tế bào trên kính và integrin nhận ra nó và bám dính vào các tế bào. Tiêu điểm bổ sung Kinase (FAK) được sử dụng trong quá trình này.
Dependent Adhesion Molecules)
Các tín hiệu bên trong và bên ngoài tác động lên Rac, Rho và cdc 42 để điều chỉnh các tiếp điểm tiêu cự (Rac, Rho và cdc 42) xác định hình dạng tế bào bởi họ protein Rho). Tín hiệu từ bên ngoài đến từ integrin để kích hoạt FAK và sau đó src (từ sarcoma) để kích hoạt tín hiệu. Tín hiệu này là tín hiệu sinh tồn. Src là kinase, serine, threonin, tvrosine axit photpho hóa cho 3 loại axit.
(2) Immunoglobulin Family (Họ Immunoglobulin)
Tên của nó tương tự như tên của immunoglobulin trong kháng thể. Gia đình ig liên kết ba chiều với liên kết disulfide thay vì canxi. Các loại bao gồm Phân tử kết dính tế bào thần kinh (NCAM), Phân tử kết dính tế bào (ICAM) và Phân tử kết dính tế bào mạch máu (VCAM). NCAM được sử dụng để liên kết kết nối các khớp thần kinh.
(3) Selectin
Selectin được đặt tên tương tự với lectin đồng thời liên kết với carbohydrate. L(leukocyte)-selectin, E(endolhelial)-selectin, P(platelet)-selectin tồn tại. P- selectin khiến các tiểu cầu tụ lại làm ngưng chảy máu và lấp đầy vết thương, p-selectin được sử dụng khi các tiểu cầu kết dính lại với nhau. Nó được tiết ra dưới dạng exocytosis của p- selectin trong alpha-granule.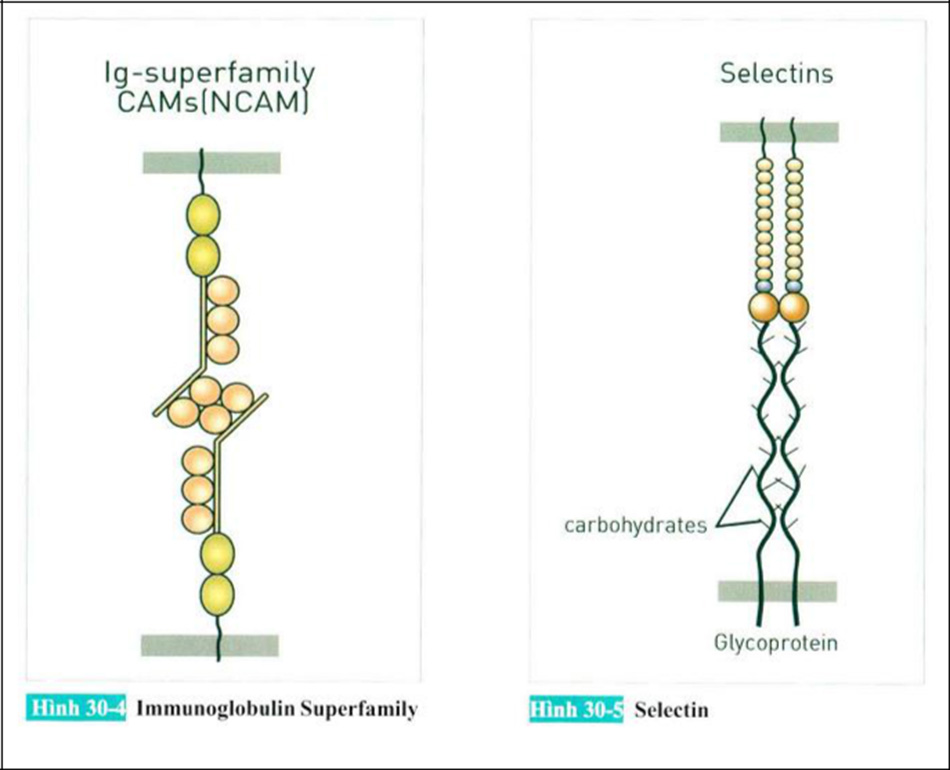
(4) Integrin
Integrin là một dimer hetero tồn tại dưới dạng kết hợp của các tiểu đơn vị alpha và beta. Có nhiều loại alpha và beta nhưng các integrins này liên kết với các protein màng có chứa các chuỗi RGD. Integrin có ái lực cao (high affinity) và ái lực thấp(low affinity) bởi các tín hiệu mã hóa bên trong, cho phép nó liên kết mạnh hoặc yếu với phối tử (ligand) bên ngoài (rơi ra trạng thái ái lực thấp). Các loại integrins tiêu biểu gồm lamini, fibronectin và fibrinogen. Vai trò của integrins rất quan trọng đổi VỚI sự tương tác của các tế bào và chất nền ngoại bào ECM.
2. Cấu trúc và sự kết nối tín hiệu của các tế bào
(1) Tight Junction (Liên kết chặt-liên kết vòng bịt)
Các tế bào có nhiều lớp với hình dạng cong giữa chúng. Tại các phần nhô ra khỏi bề mặt chúng kết hợp với nhau. Nó đóng một vai trò để giữ cho các vật liệu và ion bên ngoài không xâm nhập.
Giữa hai tế bào, các protein màng tế bào là constludin và claudin làm cho hai tế bào liên kết với nhau. Nó cũng được gọi là protein tetraspanin vì protein thâm nhập qua màng bốn lần.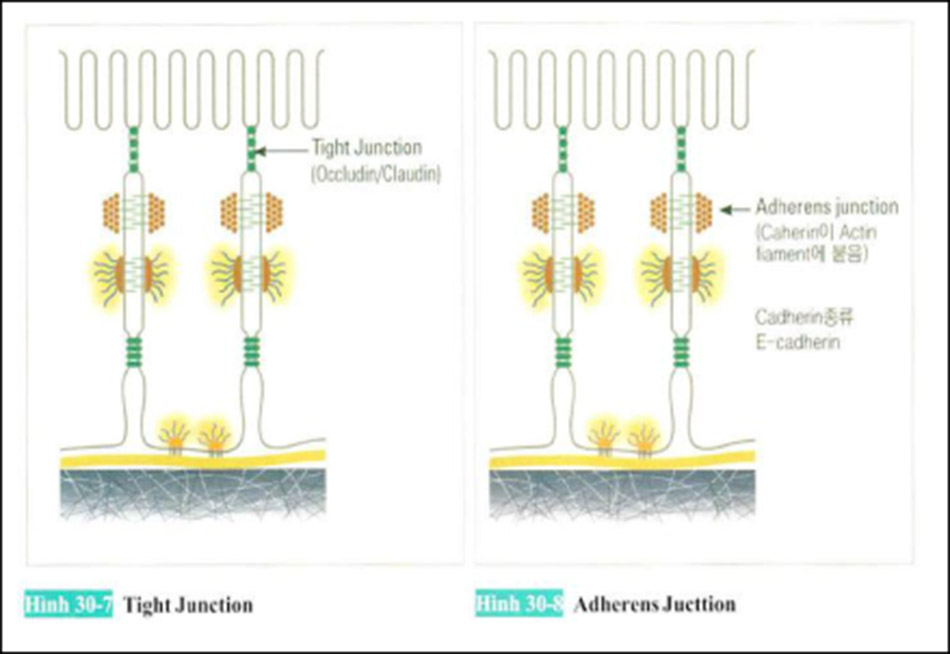
(2) Adherens Junction (Liên kết vòng)
Khi các tế bào lien kết, filopodia được hình thành, bù đắp và liên kết với nhau. Từ các phân tử trong khoảng gian bào nó neo giữ 2 tế bào biểu mô lại với nhau. Sau đó, các mối nối adherens junction được tạo ra trong hai ô này, theo đó các thế liên kết desmosome được tạo ra.
(3) Desmosome (Thể liên kết)
Cả hai đầu của desmosome có một dây intermediate filament ở desmoglein & desmocollin-một loại cadherin.
(4) Hemidesmosome (Thể bán liên kết)
Nó là một nửa của desmosome. Không giống như desmosomes, integrins được sử dụng khác hơn, nó kết hợp với Basement membrane.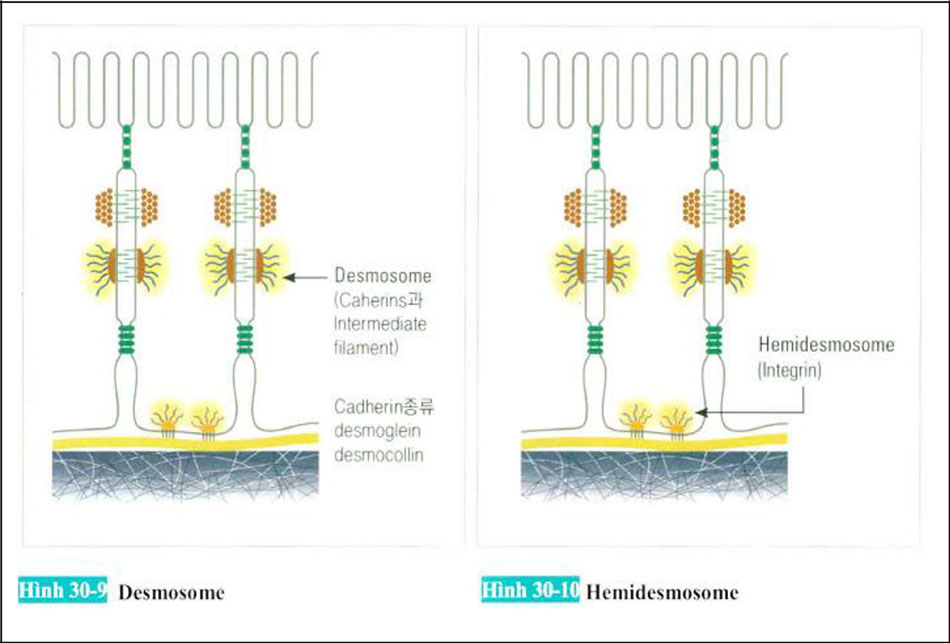
(5) Cap Junction (Liên kết khe)
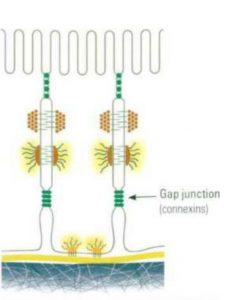
Liên kết khe (Gap junction) bao gồm một số kênh và có lỗ cho phép ra vào ion. Kênh này bao gồm 6 loại protein, connexon, mỗi loại được gọi là connexin. Connexin là tetraspanin xâm nhập qua màng bốn lần. Connexon được gọi là kênh hemi (hemi channel), phải được gắn vào để hoạt động như một kênh truyền tai.
3. Lớp thượng bì của da nhìn từ cấu trúc sinh học phân tử
(1) Sừng hóa của lớp thượng bì
Tế bào Keratinocytes, thành phần chính của thượng bì, có hình dạng khác nhau tùy thuộc vào mức độ biệt hóa và được chia thành bốn lớp. Nó được đặt tên là một lớp tế bào sừng một lớp điện cực lớp gai, một lớp tế bào mầm từ bên trong. Keratinocytes được kết nối bởi desososome và được keratin hóa để tạo ra lớp sừng.
Màng tế bào sinh học thông thường được định nghĩa là có phospholipid, sprialomyelin và cholesterol, do đó chúng hòa tan tốt trong nước hoặc hơi nước, và các vật liệu trọng lượng phân tử thấp tính thấm tốt. Nó hoạt động như một rào cản chống lại sự xâm nhập của nước và vật liệu ưa nước.
Trong tế bào sừng keratinocytes đạt đến lớp hạt và các bào quan biến mất, và profilaggrin bên trong keratohyalinegranle được chuyển thành fdaggrin sau khi phân giải protcin và khử phospho. Filaggrin này hoạt động như một chất kết dính trong tế bào, theo đó các chất trung gian keratin được sắp xếp theo chiều ngang để tạo thành macrofibrils. Trong khi đó, các ion canxi được đưa vào các tế bào để kích hoạt transglutaminase tạo ra sự liên kết không thể đảo ngược của các protein tạo nên màng keratinocyte, loricrin, keatolinin và comifin. ở phần dưới của lớp sừng, màng tế bào tạo thành một cấu trúc được bao quanh bởi màng keratinocyte chứa đầy keratin macrofibril.
Trong lớp hạt, lớp tế bào này chiếm 1% tổng thể tích, nhưng trong lớp sừng, nó chiếm khoảng 5-30%. Các lipit chính của hàng rào bảo vệ da, ceramide, cholesterol và axit béo tự do, ngày càng trở nên ngược dòng. Liên kết của keratinocytes bởi các desmosomes suy yếu.
Keratinocytes có kích thước lớn, hình dạng phẳng, được sắp xếp trong cấu trúc, nó thay đổi trong màng tế bào và các kháng nguyên và thụ thể bề mặt, nó sẽ bị phân hủy trong tế bào trong một thời gian ngắn và mất nước. Có 20 loại keratin được sản sinh trong lớp thượng bì và khoảng 10 loại trên nang tóc. Keratin loại I là K10-K20 và loại 2 là K1-K9. Keratin được ghép nối để tạo thành dạng sợi (filament), tùy thuộc vào loại tế bào, loại mô, trạng thái phát triển và biệt hóa.
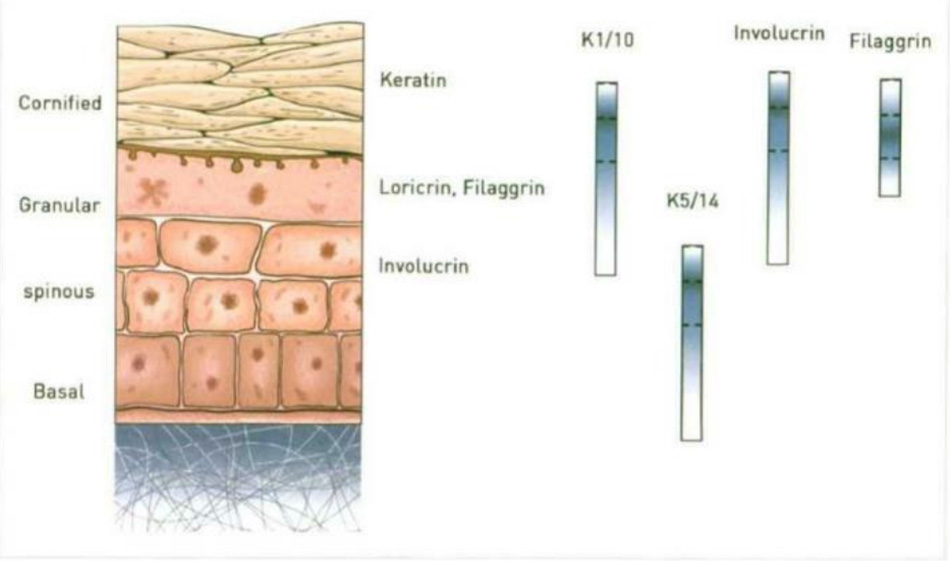
K.5 / K14 trong các tế bào cơ bản, K1 / K10 trong biểu bì gan biểu bì, K4 / K13 ở’ niêm mạc, K3 / K12 ở giác mạc, K9 keratin ở lớp cơ bản trên của bàn tay và lòng bàn chân.
Filaggrin là một chất được làm từ profilaggrin và chủ yếu ở các lớp hạt. Trong quá trình biệt hóa tế bào keratinocytes, KIF(Keratin Intennediate Filament) tập hợp lại để làm nên hình dạng của keratinocytes phẳng, từ đó tạo ra các quá trình keratin hóa và đóng vai trò duy trì hình dạng của keratin. Do đó, xét theo biểu hiện và chức năng của filaggrin một cách rõ rệt đó là một dấu hiệu cho thấy trạng thái biệt hóa của keratinocytes.
Lớp mầm tế bào sừng bao gồm các protein giàu proline các keratolinin, loricrin, và comifin, chất ức chế protein serine elafin, filaggrin-linker, peptide phân đoạn và envoplakin. Involucrin là một loại protein giàu cystein, lần đầu tiên được tạo ra trong comified envelope. Dây là một trong những thành phần phổ biến của mầm. Được biết là hoạt động như một khung giàn giáo (scaffold), nơi các protein cấu trúc khác có thể liên kết chéo.
Loricrin là một loại protein giàu lưu huỳnh, glycine / serine không hòa tan và chiếm khoảng 75% protein vỏ tế bào. Envoplakin kết nối vo tế bào (cell envelope) với sợi collagen và sợi keratin (keratin filament).
Tại spine keratinocytes chứa rất nhiều desmosome, cấu trúc quan trọng của các desmosome là các mảng bám desmosomal (desmosomal plaque) trong tế bào chất bao gồm sáu polypeptide: plakoglobin, desmoplakin I, II, keratocalmin, desmoyokin và protein band 6 (plakophilin). Các glycoprotein xuyên màng thuộc họ Cadherin bao gồm desmoglein 1 và 3 và desmcollin I và II, cung cấp sự liên kết của collagen. Các miền nội bào (intracellular domains) của glycoprotein (transmembrane glycoproteins) xuyên màng thuộc họ Cadherin (Cadherin family) được liên kết với keratin, cấu trúc của desmosome bất thường hoặc sự cố của desmosome là nguyên nhân gây phồng rộp trong lớp thượng bì. và là thiên bảo sang do sự liên kết của tự kháng thể với desmoglein 1 và 3.
(2) Lớp đáy của thượng bì
Trong số các chức năng độc đáo và thiết yếu so với các tế bào lớp cơ bản khác là sự phân chia mạnh mẽ, có chức năng hình thành màng đáy để gắn và hỗ trợ mạnh mẽ cho toàn bộ lớp thượng bì của lớp trên với mô liên kết ngoài da.
Lớp đáy thượng bì bao gồm hàng chục lớp tế bào biểu mô vảy từ lớp cơ bản đến lớp sừng, tạo thành các mô khá cứng trong cơ thể bởi hoạt động của mạng lưới sợi keratin hoặc lớp sừng của lớp tế bào. Keratinocytes thượng bì và nguyên bào sợi làm việc cùng nhau để xây dựng một cơ chế kết dính biểu bì phức tạp và tinh tế cho lớp biểu bì mỏng, mạnh để bám dính mạnh vào lớp trung bì, một thành phần tế bào mềm nhưng kém. Một lớp tế bào mỏng nhưng chắc chắn dàn trải ra linh hoạt.
Tại lớp màng đáy thượng bì bao gồm nhiều loại integrals và protein màng BP180 (BPAG2) và BP230 (BPAG1 ) / plectin sao lưu chúng trên màng đáy của tế bào đáy biểu bì nhờ vào Hemidesmosome. Proteoglycans như laminin 5 hoặc axit hyaluronic liên kết với protein esmosome hemmol, và sau đó được gắn vào các sợi collagen bao gồm collagen loại I/ III / IV thông qua collagen VI – một collagen nhỏ. Nó liên kết với collagen thành liên kết giữa lớp thượng bì mạnh và cứng và lớp trung bì.
Các tế bào lớp dáy có protein keratin 5 và keratin 14 (K5-K14) sao lưu hemidesmosome chung, bất kể loại mô não chẳng hạn như da hoặc màng nhầy, hoặc các bộ phận của cơ thể.
Các sợi Keratin (Keratin filament) xuất hiện dưới dạng cặp K5 / KI4, với các yếu tố tế bào học tương ứng với các vi chất và vi ống như actin, myosin và a-actinin.
Ngoài ra còn có các yếu tố bề mặt tế bào, là integrins cần thiết cho sự khởi đầu và biệt hóa của các tế bào. Hơn 20 thụ thể integrin tồn tại dưới dạng heterodimer. Các phân tử matrix molecule cũng có có liên quan thông qua các thụ thể integrin. Các integrin chính là ‘6 4 và 3 1. I integrin chủ yếu hiện diện ở phía tế bào keratinocytes. 6 4 được liên kết với semiglia trong lớp đáy. Integrin hoạt động như một liên kết vật lý và là con đường truyền tín hiệu giũa các phân tử cơ chất như collagen, laminin, fibronectin, thrombospondin và tronectin.
Các phân tử laminin collagen và hemidesmosome trong màng tầng hầm của lớp đáy VỚI khả năng chịu được với áp lực bên ngoài trên da.
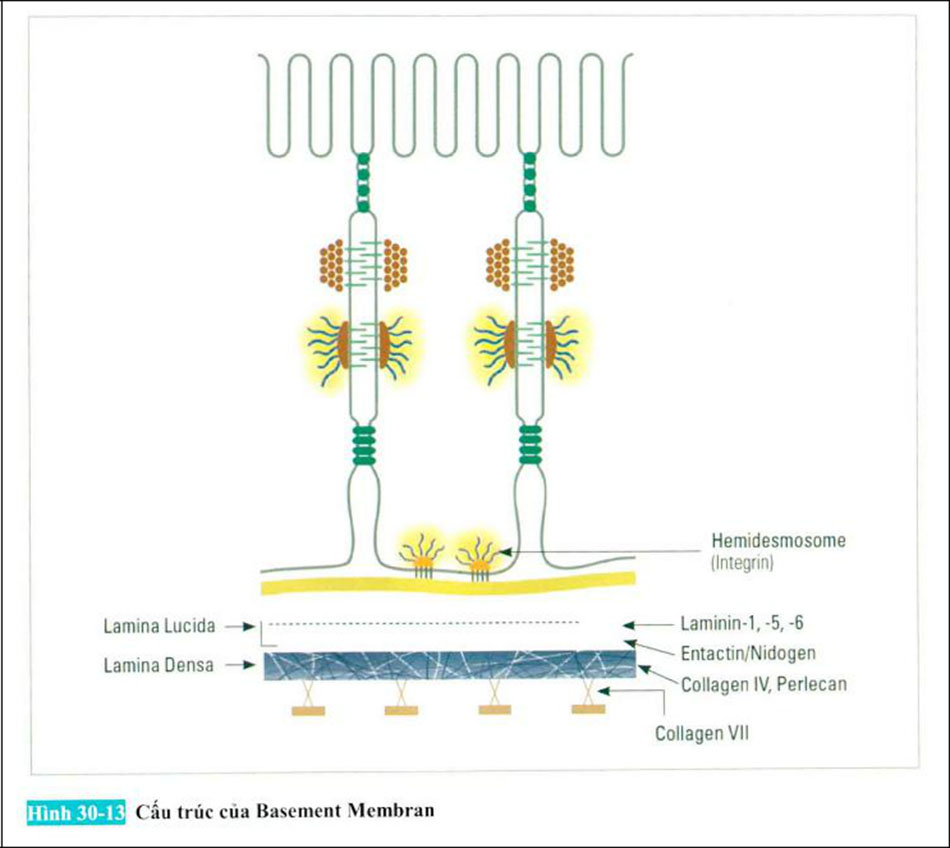
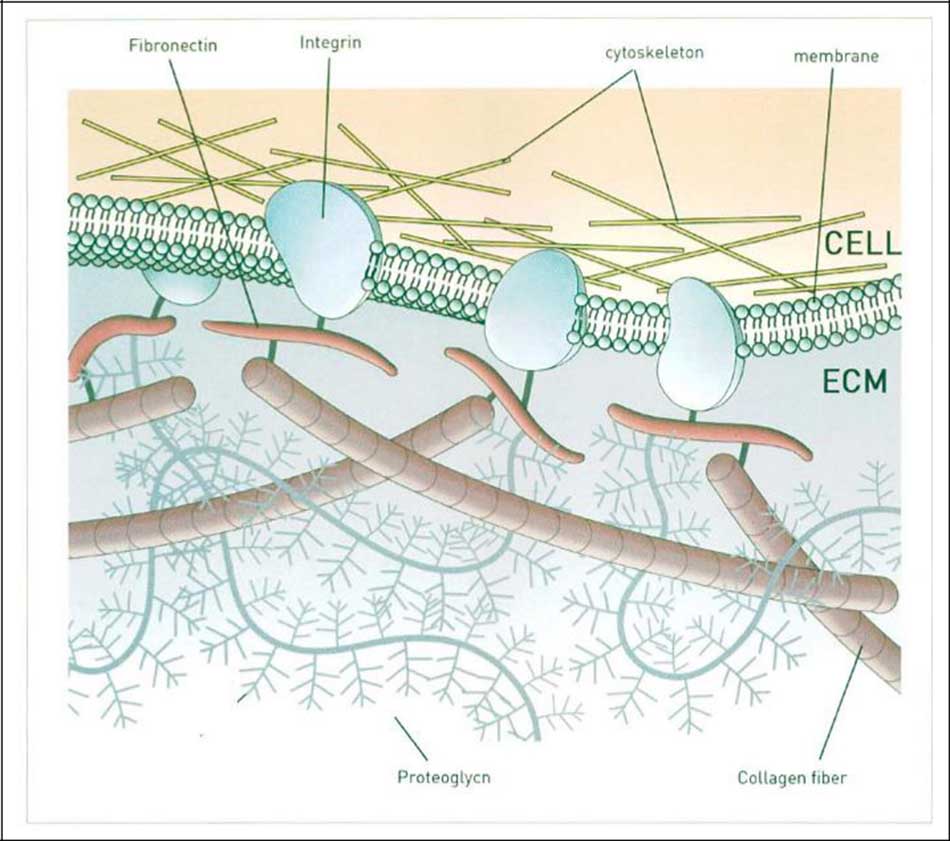
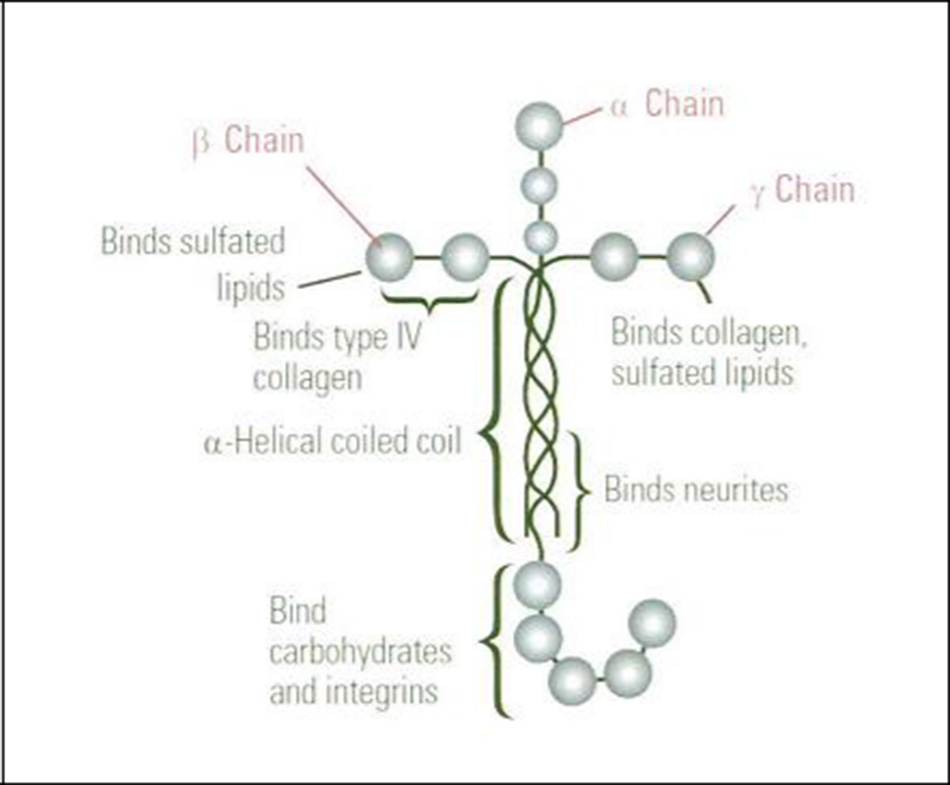
Trong trường hợp của laminin ở tại vị trí được tạo chuỗi được gọi là chuỗi ‘ (khoảng 2 triệu kDa), chuỗi và chuỗi (khoảng 4 triệu kDa) tạo thành hình chữ thập và hình thành ba chồi ngắn và một chuỗi dài để hình thành cấu trúc 3 chuỗi dưới dạng cuộn, mỗi chuỗi laminin có 1-3 vùng hình cầu và chuỗi ngắn đoạn cuối đầu N, kế tiếp hình thanh một chuỗi dài đầu đoạn c để tạo thành một cấu trúc xoắn ốc hơn nữa trong trường hợp chuỗi vùng hình cầu được nối với chuỗi tạo thành một khu vực hình cầu tại điểm cuối C.
Chức năng của mỗi miền được tìm thấy là liên kết tại điểm cuối N với ma trận khác, tại điểm cuối c và hoạt động bám dính tế bào. Trong lớp màng đáy, laminin kết hợp với các thành phần ngoại bào matrix như IV, VII, collagen loại X và Palecan để tạo thành cấu trúc giống như màng, và cũng tăng cường lớp thượng bì và trung bì. Cho đến nay 5 chủng loại chuỗi , 3 chủng loại , 3 chủng loại ‘ và 15 loại laminin được sản xuất bởi sự kết hợp của ba chuỗi này đã được tìm thấy. Mỗi laminin được phân phối và chức năng khác nhau.
4. Phản ứng chữa lành vết thương (Wound Healing Process) trong sinh học phân tử
Trong phản ứng chữa lành vết thương có 3 nhân tố quan trọng là tế bào, cấu trúc chất nền ngoại bào (extracellular matrix ECM) và cytokine khác nhau. Tổn thương mô kèm theo hiện tượng xuất huyết sẽ khiến cơ thể tiết ra catecholamine dẫn đến việc co mạch (vasoconstriction) tạm thời. Ngay sau đó dưỡng bào ( mast cell) tiết ra histamine, serotonin và bradykinin khiển mạch máu giãn nở, đồng thời huyết thanh và Protein xuyên mạch (diapedesis) . Sự kết tụ tiểu cầu (platelats aggregation) ở miệng vết thương xảy ra và điều này giúp giải phóng chất làm đông máu (clotting factors), đồng thời hình thành các tơ huyết (fibrin) giúp đông máu (coagulation) tại miệng vết thương. Hơn thế nữa tiểu cầu cũng sản sinh các cytokines thiết yếu trong việc chữa lành vết thương.
Tế bào bạch cầu(leukocytes) cũng bắt đầu xuất hiện chuyển động, trong 24 giờ đầu tiên các tế bào bạch cầu nhân đa hình (poymornuo- nuclearloukocytcs) không nhiều, tuy nhiên trong các bạch cầu monocytes các Đại thực bào(macrophges) đang phân hóa dần chiếm ưu thế. Một trong những khả năng quan trọng của đại thực bào là tiết ra các yếu tố tăng trưởng cytokines growth factors. Các yếu tố tăng trưởng đấy mạnh hoạt tính của các tế bào nội mô(endothelial cells), nguyên bào sợi(fibroblasts) và epithelia cells, giữ vai trò chủ đạo trong việc hình thành các mô hạt (granulation tissue). Việc xuất hiện bạch huyết bào (bạch cầu lympho) nhiều hơn hẳn nên tế bào lympho được suy đoán lá có liên quan đến việc tái tạo collagen (collagen remodeling) bảng cách tạo ra interlukin-1 và điều chỉnh hoạt động của enzyme collagenase.
Những thay đổi trong tế bào sừng (keratinocytes) diễn ra, lớp thượng bì (epidermis) dày lên, các tế bào đáy (marginal basal cells )phát triển và di chuyển đến vùng khiếm khuyết của vết thương. Các tế bào đáy gần vết thương liên tục phân chia và các tế bào con dần trở nên bằng phẳng và di chuyển lên miệng vết thương. Khi đó, sự kết dính glycoprotein fibronectin, vitronectin và tenascin chịu trách nhiệm Thúc đẩy sự di chuyển của các tế bào biểu mô(epithelial cells) lên miệng vết thương(migration).
Phần da gần vết thương được kéo đến phần khiếm khuyết của da theo quá trình được gọi là co rút(contraction). Nói chung, thông qua những hiện tượng này làm giảm diện tích sẹo (scar) và chữa lành khuyết điểm. Tế bào giữ vai trò chính trong sự co lại của vết thương(wound contraction) chính là myofibroblast, nhưng các thành phần cấu trúc nền (matrix components) của vết thương cũng góp phần vào sự co lại.
Myofibroblasts là một loại tế bào trung mô (smooth muscle cell) với các tính năng cấu trúc và chức năng của nguyên bào sợi và tế bào gốc trung mô mesenchymal cell. Myofibroblasts được biết là có liên quan đến quá trình co vết thương. Điều này đã được Gabbiani tiết lộ vào năm 1979, tế bào này có đặc điểm cấu trúc giữa nguyên bào sợi và tế bào cơ không chủ động (smooth—muscle cell). Cho đến ngày nay, học thuyết về sự biến đổi của nguyên bào sợi và học thuyết hoạt động độc lập của tế bào vẫn tồn tại song song, bao gồm cả vi sợi actin microfilament được sắp xếp tham gia vào quá trình co lại của vết thương. Những tế bào này sẽ xuất hiện vào khoảng ngày thứ 3 sau khi bị thương, số tế bào này đạt tối đa trong khoảng từ 10-21 ngày. Hơn thế nữa, sau khi miệng vết thương được khép lại hoàn toàn thì số tế bào này sẽ biến mất, và có mối liên hệ trực tiếp giữ mức độ lành vết thương và nguyên bào sợi.
Myofibroblast này có khả năng co cơ của Actin-myosin trong tế bào chất. Trong quá trình chữa lành vết thương, có một mối quan hệ đặc biệt giữa các tế bào và chất nền ngoại bào extracellalar matrix của tế bào. Các glycoprotein của extracellalar matrix bao gồm fibronectin, tenascin, laminin, fibrinogen, thrombospondin và vitronectin..vv. Các tế bào thông qua cell-surface adhesion recaptors được gọi là integrins thụ thể kết hợp với adhesion glycoproteins.
Trong số này, fibronectin có liên quan đến sự co rút vết thương(wound contractin), tế bào ani gratia, collagen matrix deposition và tái biểu mô hóa(re-cpithelialization). Firbronectin là một trong những protein đầu tiên được tạo ra bởi nguyên bào sợi, tế bào biểu mô và đại thực bào và đọng lại trên vết thương. Fibronectin cũng liên kết với một số phân tử tham gia vào quá trình chữa lành vết thương: collagen, actin, fibrin, axit hyaluronic, heparin, hoặc chính sợi protein và các thụ thể bề mặt tế bào trong nguyên bào sợi. Các nguyên bào sợi của mô hạt được phủ một lớp ma trận fibronectin (fibronectin matrix) , myofibroblasts cũng được phủ bằng fibronectin, Fibronexus, kết nối sợi ngoại bào và các vi chất nội bào (vi sợi nội bào- microfilaments(intracellular microfilaments) thông qua màng tế bào, hình thành sự co thắt vết thương.
Collagen bao gồm các protein có cấu trúc ba chuỗi xoắn (triple-helix) và có khoảng 13 loại collagen trong các mô khác nhau của cơ thể.
Collagen loại I, tạo thành cấu trúc chính của xương, da và gân, loại phổ biến nhất và loại II, được tìm thấy chủ yếu trong sụn, sẽ được thảo luận dưới đây.
Collagen loại III: Được tìm thấy liên quan đến collagen loại I, nhưng khác nhau về tỷ lệ tổ chức mô. Collagen loại 3, còn được gọi là collagen bào thai (fetal collagen), do có nhiều trong bào thai. Đây là collagen dồi dào thứ hai trong da người. Collagen loại 3 chiếm khoảng 50% collagen trong da thai nhi. nhưng ở người trưởng thành, collagen loại 3 chiếm khoảng 1/6 collagen loại 1. Collagen loại 3 có nhiều trong các cơ quan đàn hồi, dạ dày và động mạch chịu trách nhiệm tiêu hóa. Không giống như collagen loại 1, có hai cấu trúc chuỗi khác nhau, collagen loại 3 bao gồm cả ba chuỗi. Collagen loại 3 cũng có cấu trúc xoắn ba.
Collagen loại IV: tạo thành màng đáy (basement membrane). Collagen loại 4 có nhiều trong màng đáy phân chia lớp trung bì từ lớp biểu bì. Giống như collagen loại 1, collagen loại 4 bao gồm hai loại collagen, đó là hai chuỗi và một chuỗi. Collagen loại 4 có các amino rất lớn và carboxy (carboxy-domain) với cấu trúc xoắn ba rất ngắn. Collagen loại 4 bao gồm ba chuỗi xoắn polypeptide độc lập.
Collagen loại 7 rất đặc trưng và bao gồm ba chuỗi collagen giống hệt nhau, tương tự collagen loại 3. Các chuỗi này có cấu trúc lớn hơn các chuỗi hình thành collagen loại 1 hoặc 3. Collagen loại 7 là một cấu trúc quan trọng kết nối lớp biểu bì và lớp trung bì. Giống như collagen loại 4, collagen loại 7 cung cấp sự linh hoạt vì sự hiện diện của một vùng bị gián đoạn (interrupted region ) trong cấu trúc xoắn ba. Bệnh phồng rộp bẩm sinh nghiêm trọng (loạn sản) là một căn bệnh gây ra bởi đột biến collagen loại 7. Điều này là do kết nối sợi với sợi không xảy ra đúng cách, làm cho các sợi dễ bị đứt hơn, dẫn đến phồng rộp và chữa lành vết thương bất thường. Theo quan điểm của hiện tượng này, collagen type 7 có thể được cho là có chức năng kết nối lớp thượng bì và lớp trung bì.
Lớp trung bì bình thường chứa khoảng 80% collagen loại I và 20% collagen loại III. 24 giờ sau khi bị thương, các nguyên bào sợi xâm nhập bắt đầu tổng hợp và tiết ra collagen loại I và loại III để tạo thành một cấu trúc(matrix) mới. Các mô đang lên da non có lượng collagen loại III tĂng nhanh hơn hẳn các mô bình thường tuy nhiên dù vậy thì collagen loại I vẫn là thành phần chính trong quá trình chữa lành vết thương. Collagen bao gồm 3 chuỗi alpha-peptide gồm ba chuỗi xoắn (triple-helix). Chuỗi alpha Procollagen được tổng hợp trong các ribosome của nguyên bào sợi, và khi chuỗi alpha- peptide phát triển, chúng rời khỏi ribosome và đi vào mạng lưới nội chất thô ((rough endoplasmic reticulum). Ở đó, glycosyl hóa và hydroxyl hóa tạo thành ba chuỗi alpha- peptide (3 alpha-peptide chains), sau đó được bài tiết qua màng tế bào. Hydroxyl hóa proline được tiến hành dựa vào dioxygenases của 2 chất gọi là lysyl hydroxylase và Prolyl hydroxylase. Tại thời điểm này, các yếu tố hỗ trợ tác dụng như sắt (sắt), alpha- ketoglutarate, vitamin-c (ascorbate) và oxy (oxy) đóng vai trò rất quan trọng. Collagen chiếm phần lớn cấu trúc da và liên quan tới khối lượng và độ đàn hồi của da, cho phép da chống lại các lực tác động bên ngoài.
Collagen có nguồn gốc từ Hy Lạp ( trong Hy Lạp Collagen có nghĩa là “người sản xuất keo hồ) bởi vì khi được làm nóng, Collagen thể hiện các đặc tính tương tự như keo hồ.
Trong cấu trúc da chứa nhiều nhất collagen loại 1 và loại 3. Collagen loại 1 chiếm 80% trọng lượng trong lớp trung bì, là thành phần chính của cơ thể. Collagen loại 1 bao gồm chuỗi polypcptlde ba chuỗi, hai trong số các xoắn của collagen loại 1 có cùng cấu trúc và các sợi khác có cấu trúc khác nhau. Sự hình thành collagen được hoàn thành bằng cách di chuyển từ tế bào này sang tế bào khác theo từng giai đoạn. Collagen được tiết ra từ bên ngoài da đồng thời kéo dài ra khỏi vòng xoắn ốc, khi đó n-terminal và c—terminal domain được tìm thấy.
Các phân tử collagen được sắp xếp theo một cách rất cụ thể và hiển thị hình dạng dải trên kính hiển vi điện tử. Các dai xuất hiện ở các khoảng 68nm, đây là một phát hiện đặc trưng của collagen và xảy ra do chuỗi axit amin của các phân tử collagen. Trong collagen, glycine có mặt trong mỗi ba chuỗi axit amin, dẫn đến Gly-X-Y. X và Y chủ yếu bao gồm proline và hydorxyproline. Trong lớp trung bì, collagen loại I (60%)> loại III (15%)> loại V (dưới 5%)> loại VI tồn tại và loại IV, loại X và loại X ‘tồn tại trong màng đáy của lớp thượng bì.
Trong da, loại V cùng tồn tại với các sợi collagen như collagen I và III. Trong sụn, collagen IX và XI cùng tồn tại với các sợi collagen như collagen loại II. FACIT liên kết với các khoảng trống của collagen dạng sợi (fibril associatcd collagenes with intcrrupted triple helices) gọi là collagen FACIT collagen loại I, II, III, V và X để kiểm soát độ dày của sợi. Collagen FACIT là viết tắt của Collibrens liên kết Fibril với ba trợ giúp bị gián đoạn. Collagen FACIT được đặt trong lớp trung bì cùng với collagen loại I và giúp đảm bảo rằng collagen loại 1 được phân bố hợp lý.
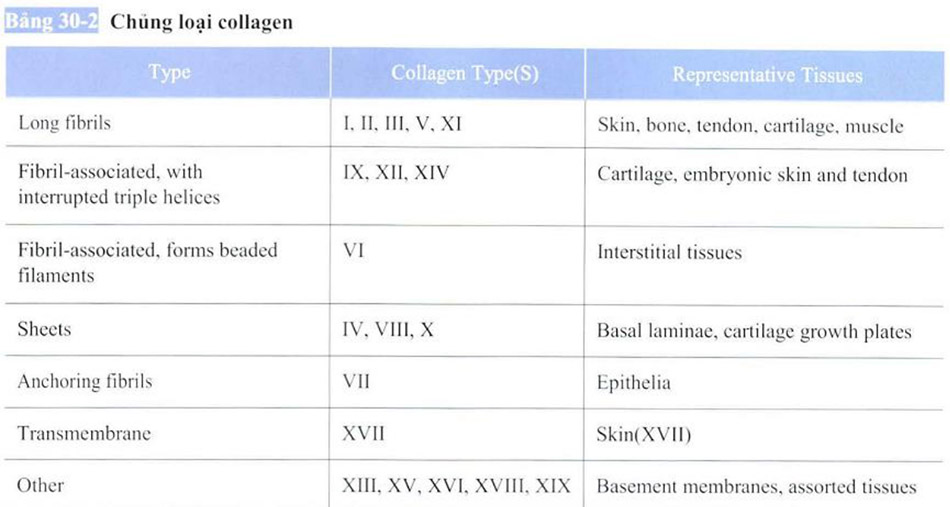
Ở vùng da không tiếp xúc, sợi đàn hồi chỉ bằng 1 đến 2% trọng lượng khô. nhưng chức năng trong da là rất cần thiết. Sợi đàn hồi có liên quan đến sự kéo căng và trở lại của da và duy trì cân bằng nội môi của da từ các lực vật lý bên ngoài. Sợi đàn hồi bao gồm các protein như bỏ đàn hồi, fibrillin và sợi xơ. Proteoglycans và glycosaminoglycans cũng được liên kết với các sợi đàn hồi. Sợi đàn hồi bao gồm các sợi đàn hồi và phần kém đàn hồi hơn bao gồm fibrillin tương ứng với protein fibrillar. Sợi đàn hồi tạo thành các cấu trúc phức tạp trong lớp trung bì. Sợi đàn hồi có trong lớp lưới của lớp trung bì có thể được quan sát nhuộm màu đến bằng nhuộm EVG. Đồng thời, nó là một sợi nhuộm màu đến, kéo dài vuông góc với đường viền của lớp biểu bì và trung bì, sợi Oxytalan được gắn vào màng đáy dưới dạng đèn chùm, tồn tại trong lớp nhú (papillary layer), và khi vào sâu hơn có các sợi elauinin nằm song song với ranh giới giữa lớp thượng bì và lớp trung bì. Đại đa số các oxytalan được hình thành bởi các sợi cực nhỏ, và được biết trong đó cũng bao gồm cả elastin nhờ vào quá trình nhuộm elastin. Tuy nhiên, lượng elastin cực kỳ nhỏ so với các sợi đàn hồi của lớp lưới, hơn thế nữa, lượng elastin cũng giảm dần và biến mất trong quá trình lão hóa.
Trong lớp lưới, có các sợi đàn hồi có độ dày 1 – 3 m giữa các sợi collagen và ngay ca ở trạng thái bình thường. Sợi đàn hồi chỉ chiếm 2% trọng lượng khô của trung bì. Các sợi đàn hồi có thể được quan sát dưới kính hiển vi điện tử bao gồm hai loại microfibers sợi và elastin không cấu trúc. Các sợi nhỏ là các sợi có mật độ cao với độ dày 10-12 m không cấu trúc, và được treo như một chuỗi xung quanh elastin với mật độ electron thấp. Thành phần của microfibrils là fibril, fibrin, microfibril liên quan đến protein và collagen loại VI. Giữa các phân tử elastin, một số lượng lớn các liên kết chéo được gọi là desmosin và isodesmocin được hình thành, và như trong hình 30-15 chúng có thể được phục hồi nhanh chóng.
Về tính đàn hồi, cả hai yếu tố liên kết ngang phân tử và liên kết tốc độ nội phân tử đều có mối quan hệ mật thiết. Trong lớp nhú, các sợi đàn hồi bao gồm các mô võng mạc mỏng manh, kéo dài vuông góc với lớp nhú và bao quanh các mạch máu. Một phần của các sợi đàn hồi kéo dài đến lớp biểu bì được tạo thành từ fibrillin và các sợi đàn hồi tương đối nhỏ. Trong lớp trung bì chính thức (trung bì sâu), các sợi đàn hồi dày hơn và được sắp xếp theo hướng song song với lớp biểu bì, tương tự như các sợi collagen. Tính đàn hồi của sợi đàn hồi được hình thành dựa trên domain của chất kỵ nước có trong aueous milieu. Các domain này do kỵ nước nên đã giảm khối lượng cấu trúc để giảm lượng nược, đồng thời làm xuất hiện tính đàn hồi có trong sợi đàn hồi. Chứng thiếu hụt sợi đàn hồi gây ảnh hưởng đến tổ chức như mạch máu hay da. Sợi đàn hồi thay đổi tính chất và độ lớn dựa vào tuổi tác. Vào độ tuổi 10 sợi đàn hồi liên tục phát triển và sản sinh tuy nhiên sau độ tuổi 20 thì lại dần dần giảm xuống. Lão hóa bắt đầu có dấu hiệu rõ ràng ở độ tuổi 30-50, sợi đàn hồi bắt đầu có dấu hiệu thoái hóa và biến mất. Các sợi đàn hồi mất tính đàn hồi của chúng bằng cách lắng đọng trong lớp trung bì dưới dạng kết tụ sau khi tiếp xúc với tia cực tím trong thời gian dài và trở nên giống như các dải cao su đã được kéo giãn hoàn toàn. Thoái hóa gây ra bởi ánh sáng mặt trời là nguyên nhân chính của quá trình quang hóa, dó là do liên kết ngang, thay đổi cấu trúc của sợi đàn hồi do tia cực tím và tăng MMP.
Glycosaminoglycans (GAG) là một chất nền không có cấu trúc, được lấp đầy các bó sợi collagen. Và không được quan sát bằng nhuộm HE, nhưng được nhuộm màu xanh lam với thuốc nhuộm màu xanh aluminian. 6 loại glycosaminoglycols là hyaluronic acid, chondroitin sulfate, dermatan sulfate, heparan sulfate, heparin, kerấtan sulfate đóng vai trò rất quan trọng trong da.
Trong số 6 loại glycosaminoglycan ngoại trừ axit hyaluronic, năm glycosaminoglycan còn lại có nhóm sulfate. Ngoài ra, tất cả các glycosaminoglycan đều có nhóm carboxyl cấu trúc. Do đó, do các nhóm sulfate và nhóm carboxyl có trong glycosaminoglycan, các glycosaminoglycan này được tích điện âm và liên kết với các phân tử nước. Glycosami noglycans có khả năng liên kết các phân tử nước nhiều hơn 1000 lần so với trọng lượng phân tử của chúng, vì vậy trong da, các glycosaminoglycan này giữ các phân tử nước, do đó giữ cho da được giữ ẩm. Glycosaminoglycan ngăn ngừa da khô và giữ ẩm cho da. Khi thành phần glycosaminoglycan giảm sẽ khiến da trở nên khô hơn.
Ở da lão hóa tự nhiên, glycosaminoglycans với các nhóm sulfate bị giảm, và trong cả lớp biểu bì và trung bì của da lão hóa, lượng glycosaminoglycans với nhóm sulfate đặc biệt giảm ở phụ nữ. Việc giảm lượng glycosaminoglycan này tỷ lệ thuận với việc giảm độ ẩm của da. Trong làn da của làn da lão hóa tự nhiên, axit hyaluronic giảm đi rất nhiều ở ca nam và nữ. Hyaluronic acid không liên kết với proteoglycan và tồn tại một mình, và có lực liên kết rất cao với các phân tử nước. Do đó, giảm axit hyaluronic có thể gây khô da.
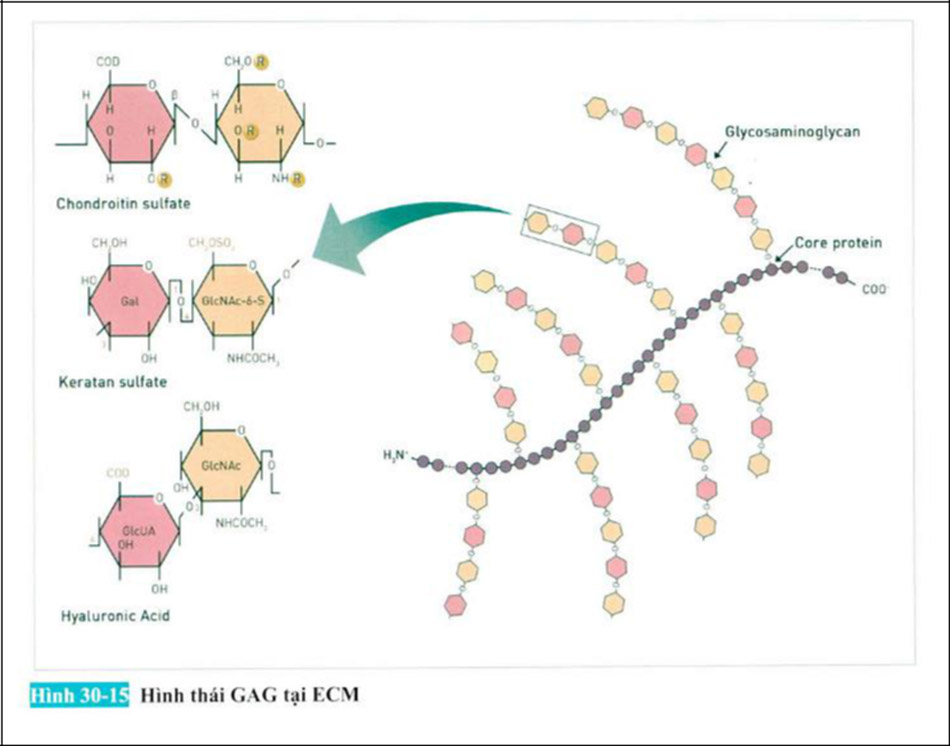
GAG có cấu trúc lặp lại của disacarit (đường amin và axit uronic hoặc galactose) với nhóm axit sunfuric được thêm vào chất gọi là mucopolysacarit có tính axit. Để tham khảo, mutin là thành phần chính của chất nhầy được tiết ra từ biểu mô động vật, có nghĩa là chuỗi đường có liên kết O-glycoside với protein lỗi (MUC). Có chức năng giữ ẩm và độ đàn hồi của da. Khi GAG giảm theo tuổi tác, độ ẩm của lớp hạ bì giảm, dẫn đến giảm độ đàn hồi của da. GAG có thể được phân loại thành proteoglycan (PG) bằng cách liên kết với axit hyaluronic và protein cốt lõi. Nhiều loại proteoglycan và protein kết hợp với nhau tạo thành mạng lưới, đóng vai trò trong việc đệm và “giàn giáo” tế bào.
Hyaluronic acid là một phần tử chuỗi tuyến tính rất lớn với 10.000 cấu trúc lặp lại disacarit của axit glucuronic và N-acetylglucosamine. Nó tồn tại dưới dạng GAG không có protein cốt lõi và vì nó có điện tích âm mạnh, nó ưa nước và có thể chứa 1000 mL nước cho mỗi 1 g. Hyaluronic acid cũng là một sự lắng đọng của chất lắng đọng ở lớp hạ bì. Nó lấp đầy giữa collagen và cũng lắng đọng giữa các tế bào nang lông. Proteoglycans (PGs) có cấu trúc trong dó một hoặc nhiều GAG được liên kết cộng hóa trị với protein cốt lõi. Việc phân loại theo hình thức phân phối của PG da có thể được phân loại như sau.
Loại magic: versican, decorin
Loại màng đáy: perlecan (pcrlecan, Có heparan sulfate trên chuỗi đường)
Loại bề mặt tế bào: Syndecan (syndecan, Matrix Receptor với Heparan Sulfate trên chuỗi đường)

Proteoglycan là tên gọi chung của họ (family name ) và bên dưới nó có một số loại, phổ biến nhất là aggrecan và verdean. Aggrecan có chondroitin sulfate, được tích điện âm yếu và thu hút nước tích điện yếu, dẫn đến áp suất thẩm thấu. Chondroitin sulfate này luôn tồn tại trong cơ thể người dù ít hay nhiều, tuy nhiên số lượng sẽ ít hơn khi già đi.
Glycoaminoglycans tạo thành proteoglycan tế bào và cùng với glycosaminoglycan tham gia vào nhiều quá trình khác nhau, chang hạn như di chuyển tế bào, duy trì hàng rào biểu bì, truyền tín hiệu quả tế bào, và hình thành sợi collagen và sợi đàn hồi. Glycosalninoglycans như axit hyaluronic cũng được sử dụng làm làm đầy cho da (derma filler).
Decorin và Versican là proteoglycan liên quan đến sợi collagen và sợi đàn hồi. Decorin là một loại chondroitin sulfate rất nhỏ hiện diện với các sợi collagen trong lớp trung bì. Decorin tham gia vào việc hình thành và duy trì các sợi collagen cùng như sửa chữa vết thương. Dermatan sulfate liên kết cộng hóa trị với protein cốt lõi trong da. Decorin liên kết với collagen để kiểm soát độ dày của sợi và do đó, làm tăng sức đề kháng và sức chống chịu của da.
Versican là một chondroitin sulfate rất lớn và được liên kết với các sợi đàn hồi trong lớp hạ bì. Versican, giống như decorin, tham gia vào việc hình thành và duy trì các sợi đàn hồi. Nó đặc biệt hiện diện trong sữa mẹ, xung quanh nang lông và màng đáy adnexal. Glute trong tim là frteoglycan với 10-20 chuỗi chơndroitin sulfate và dermatan sulfate. Nó kết hợp với axit hyaluronic ở đầu N đề tạo thành phức chất ma trận trong các sợi khác tại đầu C (tenenesine, fibrin, fibrillin, v.v.)
Fibronectin là một glycoprotein có chức năng đa dạng, bao gồm các khiếm khuyết tế bào và di chuyển trong lớp trung bì. Pibronectin có trình tự axit amin đặc biệt, trình tự RGDS, theo thứ tự arg-gly-asp-ser. Fibronectin được liên kết với các sợi collagen trong lớp trung bì.
Xem thêm
CÁC HOẠT CHẤT CHỐNG LÃO HÓA TRONG MỸ PHẨM
PHƯƠNG PHÁP GIẢM ĐAU TRONG TIÊM CĂNG BÓNG